Dne
5. září informoval Státní ústav pro kontrolu léčiv o závadě v jakosti minimálně
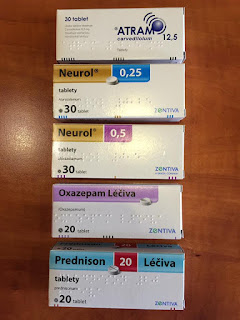
jedné (ale až tří šarží) pro 5 léčivých přípravků Atram, Neurol (dvě různé
síly), Oxazepam a Prednison.
Celkem 8
šarží a zhruba 60 000 balení. Zjištěná závažnost rizika byla důvodem pro rozhodnutí
stáhnout uvedené vadné šarže všech výše uvedených přípravků až z úrovně
pacientů a dalších 50 000 balení ze zdravotnických zařízení. Celkem 110 000 balení pouze v České
republice a dalších zhruba 1 milion 800 tisíc v evropském měřítku. Pojem „závada
v jakosti“ je v informaci SÚKL vysvětlen větou: „…je možné, že balení
bude obsahovat jiný lék, než jaký mu byl původně vydán.“
Co
takové eufemické vysvětlení znamená v praxi a jak rozumět odůvodnění?
V praxi
to znamená, že nikdo není schopen odhadnout, jaké účinné látky jsou
v tabletách toho, kterého léčivého přípravku. A možných kombinací záměn
může být mnoho. Od relativně málo rizikové záměně alprazolam/oxazepam nebo
alprazolam 0,25mg/alprazolam 0,5mg až
k významně rizikovější záměně čehokoliv za prednison. Zejména
v případě užívání některého z benzodiazepinů namísto prednisonu lze
zjednodušeně říci, že se pacient sice může cítit lépe, ale objektivně dojde
k výraznému zhoršení zdravotního stavu vlivem náhlého vysazení prednisonu,
což může vést až adrenální krizi.
Bohužel,
z doplňující informace SÚKL vyplývá, že ke dni 13. 9. byla
v souvislosti s uvedenou závadou v jakosti nahlášena celkem čtyři upozornění na nežádoucí účinek
přípravku PREDNISON a tři upozornění
pro přípravek NEUROL (alprazolam).
A
právě pro závažnost možné (a teď i pravděpodobnější) záměny
alprazolam/prednison je doporučení pacientům k návštěvě lékárny a výměně
vadné šarže za bezvadnou (respektive za tu, která se ještě nestahuje), alespoň
pro mě, nedostatečné. SÚKL sice na posledním místě informace pro pacienty
navrhuje kontakt s ošetřujícím lékařem, ale podle mého názoru by to měla
být informace primární.
Veškerá
zodpovědnost a opatření k nápravě jde k tíži držitele rozhodnutí o
registraci a nabízí se otázka, zda neměl při sběru a výměně vadných balení postupovat
razantněji, tedy pasivně nespoléhat pouze na rozhodnutí pacientů, kteří se o
tom samozřejmě ani nemuseli dozvědět. Ano, bylo by to dražší než 100 korun,
které lékárně nabízí za náklady spojené s administrativou, výměnou a
likvidací každého balení, které pacienti do lékárny donesou.
Obava,
že by se do českých lékáren vrátila od pacientů většina z 60 000
balení vadných šarží, přitom není úplně na místě. V českých lékárnách byly léky
z těchto šarží vydávány pacientům už na přelomu března a dubna tohoto
roku. Že by ve větším měřítku zůstaly i po půl roce nespotřebované, je málo
pravděpodobné a proto zdůvodnění mohlo být i v preténiu: „…je možné, že balení obsahovalo jiný lék, než jaký mu byl původně
vydán.“
O
to je celý případ závažnější. Našla se chyba, kterou lze odčinit pouze zčásti. Velká
část tablet s rizikem záměny byla již užita a to pacienty nejvíc děsí.
Nevědomost a nedostatek informací, protože je nikdo nekontaktoval, aby jim
sdělil, co za co bylo vyměněno a v jakém množství a co se mohlo stát.
Jestli je „chyba vzniklá přímo u
výrobce v rámci výrobního procesu“, jak jí označil
SÚKL ve svém avízu, spíše malého rozsahu a týká se několika tablet, které,
nedopatřením nebo liknavostí pomocného personálu (nebo zlým úmyslem), změnily
násypku pro balící linku. Nebo byl vadný celý proces a pak to postihlo celou šarži (nebo všechny)
v plném rozsahu a nesprávně a nebezpečně se v tomto případě léčil
každý z pacientů? To jsou informace, které postrádají nejenom pacienti,
ale i lékárníci, kteří by jim při výměně měli poskytovat informace,
případně uklidnění. Jenomže ani lékárníci informace nemají. Pouze domněnky
vyčtené mezi řádky šetrně dávkovaných informací.
Je
to delší doba, za půl roku si na případné potíže mnoho pacientů ani nevzpomene,
natož aby je dali do souvislostí, a i kdyby, důkazy se budou hledat jen těžko.
Přesto, nebo právě proto, se nedivím rozhořčeným komentářům pacientů na
sociálních sítích, i když hrozby žalobou proti výrobci (zveřejněné tamtéž) beru
s velkou rezervou. Jak je ze sdělovacích prostředků a médií zřejmé, jsou pochybení
farmaceutických firem častá a relativně často jsou následně i námětem pro mnohá
filmová zpracování. V nich vždycky firma mlčí, mlží a k případnému
finančnímu odškodnění přistoupí až pod tíhou soudního rozhodnutí, které se
vleče řadu let a desetiletí. Proč by to u nás mělo být jinak.
A
jak u nás na takovou minelu farmaceutického průmyslu pamatuje zákon?
Držitel
rozhodnutí o registraci a v tomto případě zároveň výrobce musí (podle §33
odst. 1, písm. e) zákona č. 378/2007 Sb., o léčivech) provést opatření k zajištění možnosti výměny léčivého přípravku pro
pacienta kteroukoli lékárnou za léčivý přípravek bez takové závady v jakosti.
Provozovatel
lékárny je pak povinen (podle §23 odst. 1, písm. e) téhož zákona) provést
veškerá potřebná opatření, a to v rozsahu a způsobem, který držitel rozhodnutí
o registraci provozovateli sdělí.
Dalo
by se říci, že pro tento konkrétní případ se provozovatelé všech lékáren
stávají (podle § 89, odst. 3) partnerem držitele rozhodnutí o
registraci/výrobce přímo ze zákona, když „postupují při odevzdávání
nepoužitelných léčivých přípravků podle pokynů držitele rozhodnutí o
registraci, který je povinen jim uhradit prokázané náklady vzniklé při takovém
odevzdávání, případně náklady vzniklé v souvislosti s pořízením a uskladněním
odevzdávaného léčivého přípravku“.
Pokud
tedy výrobce musí zajistit výměnu v každé lékárně a za to jejich
provozovatelům uhradit oprávněné náklady, přitom se může prokazování oprávněných
nákladů ukázat jako další práce a prodražení celé operace, a paušální úhrada ze
strany výrobce může být dobrým řešením a snížením jeho nákladů stejně jako
zjednodušením pro všechny účastníky. Nabízená paušální náhrada ale musí být
v takové výši, která odpovídá závažnosti a pracnosti, kterou při snižování
rizika a „odčiňování chyby“ odvádějí za výrobce lékárníci.
Jedním
ze základních pravidel by přitom mělo být kontaktování každého pacienta,
kterému byl takovýto vadný (rizikový) léčivý přípravek vydán. Lékárníci, kterým
na jejich pacientech záleží, to udělali i přes to, že takový pokyn řešení
výrobce neobsahovalo. Proč taky, mohlo by se najít víc informovaných a
potenciálně poškozených. Lze z toho usuzovat, komu na pacientech záleží a
snad to pacientům (a nejenom těm ohroženým) ukáže, že tuhle roli lékárníka není
schopen nahradit nikdo jiný v systému zdravotní péče.
Návrh
na paušální částku ve výši 100 Kč se ani neblíží míře zodpovědnosti, hodnotě
práce a vynaložené energie lékárníků. Navíc ignorování potřeby toho
základního kontaktu s pacienty vypovídá i o způsobu, jakým farmaceutické
firmy na pacienty nahlížejí.
A
pokud budu spekulovat o globální bezpečnosti, nejsou jejím nositelem pouze
vrcholní manažeři a dokonale auditované standardní protokoly. Mnohdy jsou
nejrizikovějším faktorem prosté lidské chyby nebo zlomyslnosti nedoceněných
nebo špatně vybraných obyčejných lidí na pozicích uklízeček nebo technického
personálu, kteří jako jednotlivci zůstávají pod rozlišovací schopností manažerů
vnímajících pouze cílovou skupinu.
V posledních
měsících a letech jsou, možná s rostoucím tlakem na snižování cen, možná s postupující
globalizací, podobné případy zjištění závad v jakosti léčivých přípravků
s následným stahováním až z úrovně pacientů častější než
v minulosti. S mírnou nadsázkou se postupně sestávají jednou
z rutinních lékárenských činností.
A
rostoucí frekvence a míra těchto příhod ukazuje nejen slabiny v současném
systému varování, ale také znovu otevírá otázky, které nebyly uspokojivě
vyřešeny v žádné legislativní úpravě zákona o léčivech za posledních deset
let. Chceme-li zajistit pacientům maximální míru bezpečí, je třeba je umět
rychle kontaktovat. Ještě pamatuji, když se telefonní číslo na pacienta
vyhledávalo ve Zlatých stránkách podle jména a adresy uvedené na receptu. Dnes
už to není možné a kvůli snižování rizik by mělo být kontaktní telefonní číslo
standardní součástí receptu.
V současné
době totiž do lékárny přijde pacient řešit závadu v jakosti pouze, když se
o závadě dozví ze stránek SÚKL a následně (a se zpožděním) z médií, pokud
se taková zpráva v médiích objeví. Jako standardní formu přijatých
opatření (podle ustanovení zákona) by ale měl držitel rozhodnutí o registraci
komunikovat podobnou situaci v médiích sám od sebe a to včetně odhadu
rizika. Stejně tak by mělo úplně automaticky (na náklady výrobce/držitele
rozhodnutí o registraci) docházet ke kontaktu lékárníka s pacientem. Nikdo
jiný než lékárník totiž neví, jaké množství a kterou konkrétní šarži si pacient
z lékárny odnesl.
Celý
proces by měl probíhat pokud možno automaticky a tak rychle (okamžitě) od
vyhlášení závady, aby se riziko minimalizovalo také o prodlevu, ke které
dochází při čekání na informace.
K tomu
je do budoucna vhodné upravit zákon o léčivech o povinnost uvádět kontaktní
telefon na pacienta na receptu a případně také o povinnost informovat pacienty
pro držitele rozhodnutí o registraci. Vyčíslit skutečné náklady na odpovídající
(a nikoliv urážející) částku a vypracovat standardizovaný postup aplikovatelný
na všechny případy (nebo jejich většinu) bez ohledu na osobu držitele
rozhodnutí o registraci je úkol pro profesní organizaci, regulační autoritu a
zástupce farmaceutického průmyslu.
Samostatnou
kapitolu k řešení ještě tvoří tvorba stejného postupu a vyčíslení nákladů
pro případy, kdy se léčivé přípravky stahují a vyměňují v lůžkových zdravotnických
zařízeních.
Psáno pro Medical Tribune 9. 9. 2016
Komentáře
Okomentovat